2025年10月16日�,西南大學(xué)李翀教授�����、美國(guó)俄亥俄州立大學(xué)Robert J. Lee等合作者在期刊《Nature Communications》上發(fā)表題為"Virus-inspired lipopeptide-derived nucleic acid delivery to cartilage for osteoarthritis therapy"的研究論文����。

文中使用蘇州艾特森制藥設(shè)備有限公司MPE-L2型微流控制備儀制備了一系列非致病性����、受病毒啟發(fā)的脂肽基納米顆粒(Virus-inspired lipopeptide-based nanoparticles,VPN)���,向軟骨遞送核酸����,用于骨關(guān)節(jié)炎治療�����。

研究背景
軟骨靶向基因治療在骨關(guān)節(jié)炎(OA)治療中具有良好前景���,但其療效嚴(yán)重依賴于遞送載體的有效性��,本文研究團(tuán)隊(duì)開(kāi)發(fā)了一種非致病性��、模塊化設(shè)計(jì)的病毒啟發(fā)脂肽基納米顆粒(VPN)���,并結(jié)合ROS響應(yīng)型凝膠系統(tǒng)(si-VPN@HA)��,以構(gòu)建高效安全的軟骨靶向核酸遞送平臺(tái)�����,突破現(xiàn)有OA基因治療的遞送瓶頸����。
1.VPNs與si-VPNs的設(shè)計(jì)與構(gòu)建
? VPNs的制備:脂肽自組裝:
通過(guò)固相肽合成法制備含Col2靶向頭部��、可變精氨酸/組氨酸陽(yáng)離子部分及C??疏水部分的脂肽�,將脂肽溶于DMSO后緩慢加入DEPC,攪拌10分鐘�,利用脂肽自組裝形成納米顆粒。
? si-VPNs的制備:siRNA負(fù)載:
采用艾特森微流控設(shè)備�����,將等體積預(yù)設(shè)N:P比的VPN溶液與siRNA溶液均勻混合,借助靜電吸附作用使siRNA負(fù)載于VPN 形成復(fù)合物��。

圖例1:si-VPNs制備過(guò)程
2. VPNs與 si-VPNs的制備與表征
研究團(tuán)隊(duì)成功制備了在酸性環(huán)境下可調(diào)整尺寸和電荷�����、因而更易滲透軟骨的VPN納米顆粒���。通過(guò)微流控制備方法��,VPN可以高效包裹siRNA形成si-VPN���,后者不易被酶降解�����。VPN是空心囊泡��,包裹siRNA后變成實(shí)心小球����。

圖例2:VPNs與 si-VPNs的制備與表征
3. 體外轉(zhuǎn)染與RNA干擾效能
研究團(tuán)隊(duì)發(fā)現(xiàn),在軟骨細(xì)胞中��,si-VPN-2(–[(R)5-(H)4]2–)比傳統(tǒng)載體(如MC3-LNP)攝取效率更高;在軟骨小球模型中����,si-VPN-2能穿透到小球中心,其他載體多停在表面�; si-VPN-2 能高效沉默MMP-13,可發(fā)揮基因治療作用����。

圖例3:體外轉(zhuǎn)染與RNA干擾效能
4. MMP-13沉默影響體外基因表達(dá)譜
研究團(tuán)隊(duì)進(jìn)一步驗(yàn)證了si-VPN-2臨床應(yīng)用前景,證實(shí)在患者原代軟骨細(xì)胞中���,si-VPN-2的細(xì)胞攝取效率高(較傳統(tǒng)MC3-LNP高3倍多)���,無(wú)聚集,可高效實(shí)現(xiàn)溶酶體逃逸����,使MMP-13 高效表達(dá)沉默;通過(guò)基因測(cè)序發(fā)現(xiàn)����,si-VPN-2能調(diào)控OA相關(guān)基因,影響 OA關(guān)鍵通路�。

圖例4:MMP-13沉默影響體外基因表達(dá)譜
5.納米-凝膠si-VPN@HA的構(gòu)建����、釋放與關(guān)節(jié)滯留
基于上述研究成功�����,研究團(tuán)隊(duì)構(gòu)建了一種ROS響應(yīng)型 si-VPN@HA 納米凝膠���,該凝膠可根據(jù)環(huán)境ROS水平響應(yīng)性釋放釋放 si-VPN-2��;釋放的si-VPN-2仍有高軟骨穿透能力����。si-VPN@HA可在關(guān)節(jié)內(nèi)滯留超21天���,調(diào)和了穿透和滯留的困境�����。

圖例5:納米-凝膠si-VPN@HA的構(gòu)建、釋放與關(guān)節(jié)滯留
6. 在外科ACTL模型中通過(guò)si-VPN@HA治療緩解軟骨變性
研究團(tuán)隊(duì)在在ACLT OA小鼠模型中證實(shí)si-VPN@HA的作用效果:
?較 si-VPN-2�����、si-MC3-LNP 更能減輕軟骨退變,OARSI 評(píng)分接近假手術(shù)組���;
?可實(shí)現(xiàn)約75% MMP-13體內(nèi)沉默�,下調(diào)NGF�����、MMP-9等信號(hào)���,緩解疼痛與軟骨分解����;
?調(diào)節(jié)巨噬細(xì)胞表型(減M1�、增M2)并降低炎癥基因,且安全性良好���。
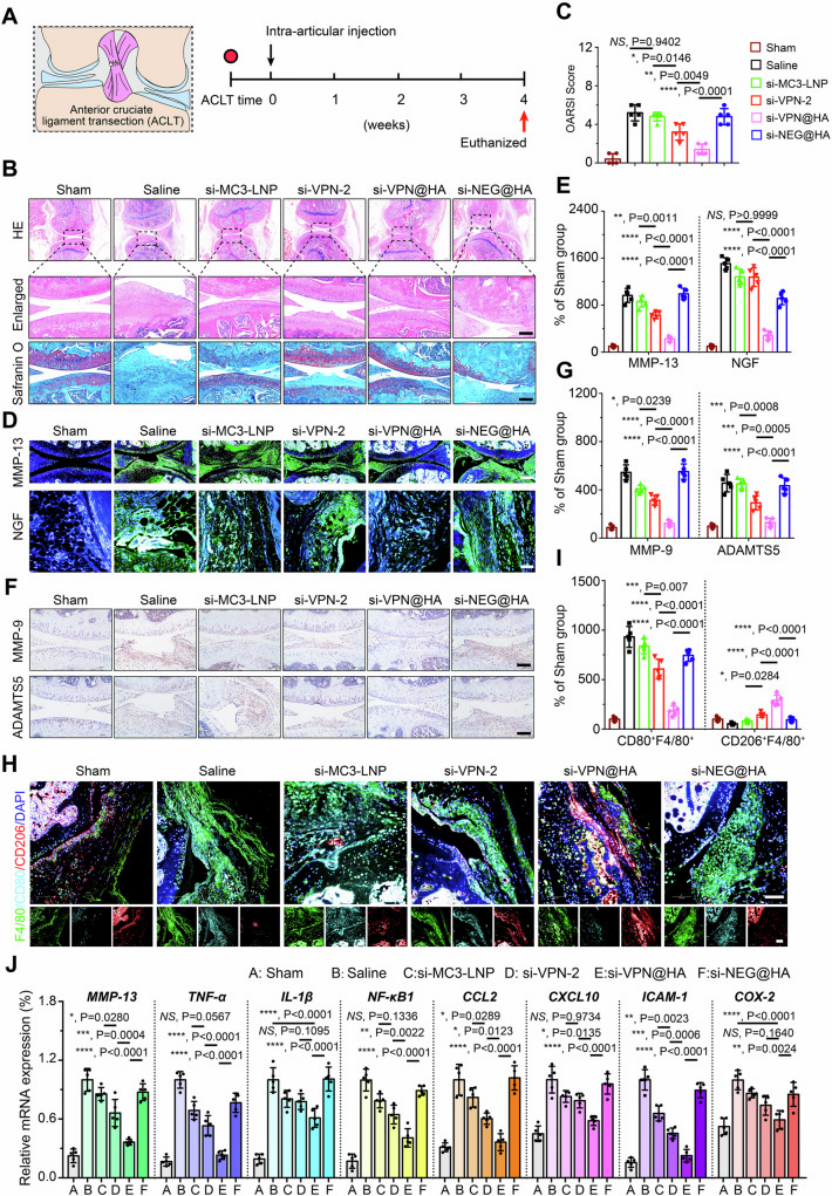
圖例6:在外科ACTL模型中通過(guò)si-VPN@HA治療緩解軟骨變性
7. PTOA模型與類固醇協(xié)同治療實(shí)現(xiàn)更優(yōu)關(guān)節(jié)保護(hù)
證實(shí)在PTOA小鼠模型中: si-VPN@HA與內(nèi)固醇合用更能保護(hù)關(guān)節(jié)功能��,減輕軟骨退變與骨贅形成�����。

圖例7:PTOA模型與類固醇協(xié)同治療實(shí)現(xiàn)更優(yōu)關(guān)節(jié)保護(hù)
8. 關(guān)節(jié)內(nèi)mRNA遞送的功能驗(yàn)證
進(jìn)一步地����,研究團(tuán)隊(duì)使用微流控制備儀將VPN與mRNA混合,制備含mRNA的納米顆粒即m-VPNs�����,證明m-VPN-2的體外轉(zhuǎn)染效率�����、體內(nèi)軟mRNA遞送效果均顯著優(yōu)于m-VPN-1及m-MC3-LNP��。

圖例8:關(guān)節(jié)內(nèi)mRNA遞送的功能驗(yàn)證
知識(shí)分享:研究亮點(diǎn)
1 本文創(chuàng)新設(shè)計(jì)出受病毒啟發(fā)的模塊化脂肽基納米顆粒(VPN)�����,以含可變精氨酸/組氨酸的陽(yáng)離子部分為核心功能組件���,優(yōu)化后的VPN-2轉(zhuǎn)染效率較傳統(tǒng)脂質(zhì)納米顆粒提升約2.5倍����,且具備pH敏感性與軟骨靶向性����,可高效遞送核酸至軟骨細(xì)胞并實(shí)現(xiàn)溶酶體逃逸。
2 為解決關(guān)節(jié)內(nèi)遞送的 “穿透-滯留” 矛盾��,構(gòu)建ROS響應(yīng)型si-VPN@HA凝膠內(nèi)納米系統(tǒng)�,該系統(tǒng)在OA高ROS環(huán)境下可釋放si-VPN-2,在ACLT小鼠中減輕軟骨退變����,與甲潑尼龍聯(lián)用還能在PTOA小鼠中實(shí)現(xiàn)更優(yōu)關(guān)節(jié)保護(hù)。
3 研究同時(shí)驗(yàn)證VPN-2可作為mRNA遞送載體��,在體外細(xì)胞與ACLT小鼠體內(nèi)均展現(xiàn)出優(yōu)異的mRNA轉(zhuǎn)染效果�����,證實(shí)其作為軟骨靶向核酸遞送平臺(tái)的通用性��,為骨關(guān)節(jié)炎創(chuàng)新治療提供新策略�。
參考文獻(xiàn):
Nature Communications (IF 15.7) Pub Date:2025-10-16, DOI:10.1038/s41467-025-64212-5
 歡迎來(lái)到蘇州艾特森制藥設(shè)備有限公司網(wǎng)站!
歡迎來(lái)到蘇州艾特森制藥設(shè)備有限公司網(wǎng)站! 歡迎來(lái)到蘇州艾特森制藥設(shè)備有限公司網(wǎng)站!
歡迎來(lái)到蘇州艾特森制藥設(shè)備有限公司網(wǎng)站!









