2025年7月1日 �,上海交通大學(xué)章雪晴團(tuán)隊(duì)與新澤西理工學(xué)院許曉陽團(tuán)隊(duì)在期刊《Nature Communications》上發(fā)表題為" Budesonide-incorporated inhalable lipid nanoparticles for antiTSLP nanobody mRNA delivery to treat steroid-resistant asthma "的研究論文。

研究團(tuán)隊(duì)使用艾特森MPE-L2型微流控制備儀制備mnbTSLP-iLNP納米粒����,經(jīng)霧化吸入肺部后,借助膜融合和GR介導(dǎo)的內(nèi)吞作用進(jìn)入細(xì)胞�����,逃離溶酶體后釋放 mnbTSLP和布地奈德�����。mnbTSLP在體內(nèi)翻譯為nbTSLP����,中和氣道過量TSLP�����,抑制STAT3和p38磷酸化,恢復(fù)布地奈德敏感性�,GR復(fù)合物入核調(diào)控炎癥基因轉(zhuǎn)錄,協(xié)同改善哮喘癥狀�。

研究背景
本研究創(chuàng)新構(gòu)建甾體結(jié)構(gòu)化的新型吸入式LNP遞送系統(tǒng),通過布地奈德等甾體分子與脂質(zhì)骨架的疏水嵌合設(shè)計(jì)���,實(shí)現(xiàn)編碼抗胸腺基質(zhì)淋巴細(xì)胞生成素(TSLP)納米抗體mRNA(mnbTSLP)的肺靶向吸入遞送�,實(shí)現(xiàn)了甾體抗炎藥物與抗體藥物在肺部的靶向富集及協(xié)同作用�。通過調(diào)控氣道炎癥微環(huán)境與阻斷TSLP介導(dǎo)的2型炎癥通路,為重癥難治性哮喘提供兼具快速起效與免疫調(diào)節(jié)優(yōu)勢的創(chuàng)新治療方案����,克服重癥哮喘中糖皮質(zhì)激素耐藥的挑戰(zhàn)。
1.ASCEND(替代類固醇與mRNA編碼納米體共同遞送)療法作用機(jī)制示意圖

圖例1:si-VPNs制備過程
? mnbTSLP-iLNP制備工藝:

圖例2:mnbTSLP-iLNP制備工藝
2. mRNA-iLNP制劑的制備與篩選
研究團(tuán)隊(duì)通過制備不同布地奈德摩爾占比(0%�����、5%����、9.5%、14%���、19%)的iLNP �����,對比霧化前后粒徑�、PDI、zeta電位及包封效率����,發(fā)現(xiàn)5%布地奈德組(iLNPBUD5)霧化后穩(wěn)定性最佳,體外轉(zhuǎn)染BEAS-2B細(xì)胞的EGFP陽性率最高(約72%)���,且轉(zhuǎn)染效率依賴GR介導(dǎo)的內(nèi)吞作用����。體內(nèi)實(shí)驗(yàn)顯示����,iLNPBUD5在肺部靶向性強(qiáng),熒光信號顯著高于其他制劑及ALC-0315對照組�,這些結(jié)果表明,含5%BUD的LNP(mRNA-iLNPBUD5)的理化穩(wěn)定性和遞送效率佳��。

圖例3:霧化遞送用 mRNA-iLNP 制劑的制備與篩選
3. mRNA-iLNPBUD5的霧化遞送特性表征
接著����,研究團(tuán)隊(duì)進(jìn)一步驗(yàn)證iLNPBUD5的關(guān)鍵遞送性能。冷凍電鏡顯示其霧化前后均為球形����、粒徑均一;4℃儲存30天仍保持膠體穩(wěn)定性�����,在中性和弱酸性生理環(huán)境中結(jié)構(gòu)穩(wěn)定�����。體外黏液滲透實(shí)驗(yàn)表明��,iLNPBUD5介導(dǎo)的mRNA穿透效率顯著高于游離mRNA����;16HBE細(xì)胞溶酶體逃逸實(shí)驗(yàn)顯示,mRNA在4小時(shí)內(nèi)從溶酶體釋放至細(xì)胞質(zhì)��,轉(zhuǎn)染后呈現(xiàn)強(qiáng)且均一的EGFP表達(dá)���,且無細(xì)胞毒性��。這些結(jié)果表明��,mRNA-iLNPBUD5具有良好的穩(wěn)定性�����、對霧化誘導(dǎo)損傷的耐受性��、良好的黏膜穿透性�、轉(zhuǎn)染效率高,以及良好的安全性�����,是一種有前景的可吸入mRNA治療載體���。
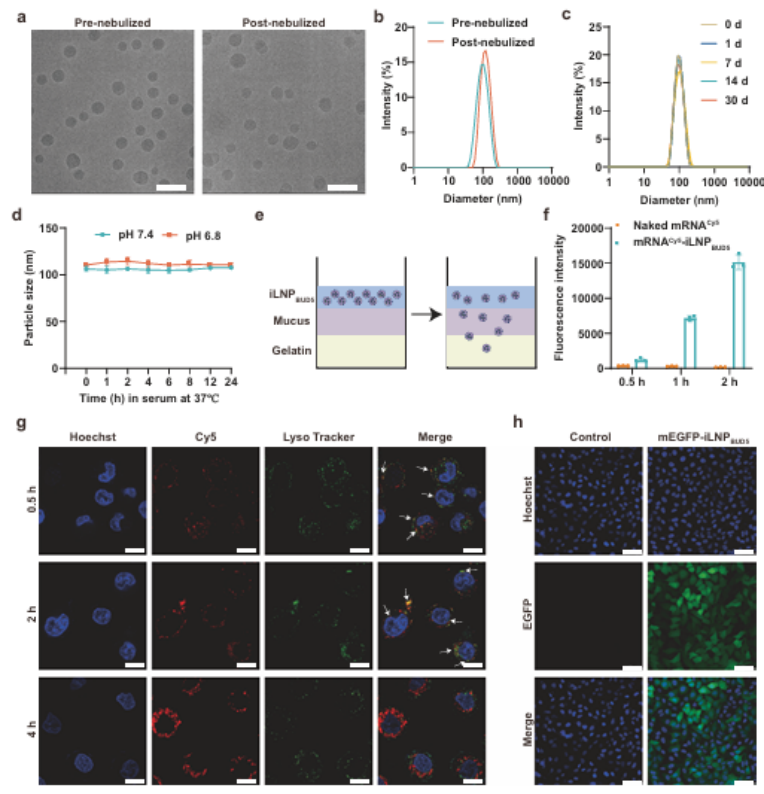
圖例4:mRNA-iLNPBUD5的霧化遞送特性表征
4.mnbTSLP的設(shè)計(jì)與體外功能驗(yàn)證
隨后��,研究團(tuán)隊(duì)進(jìn)行了mnbTSLP的序列設(shè)計(jì)和體外驗(yàn)證�����。瓊脂糖凝膠電泳和WB實(shí)驗(yàn)結(jié)果表明mnbTSLP編碼抗TSLP納米抗體���,iLNPBUD5可保護(hù)其免受血清降解����,介導(dǎo)nbTSLP劑量/時(shí)間依賴型表達(dá)��;nbTSLP與TSLP高親和力結(jié)合����,顯著抑制炎癥因子表達(dá)�����,這為治療實(shí)驗(yàn)中確定最佳給藥間隔提供了有價(jià)值的見解����。
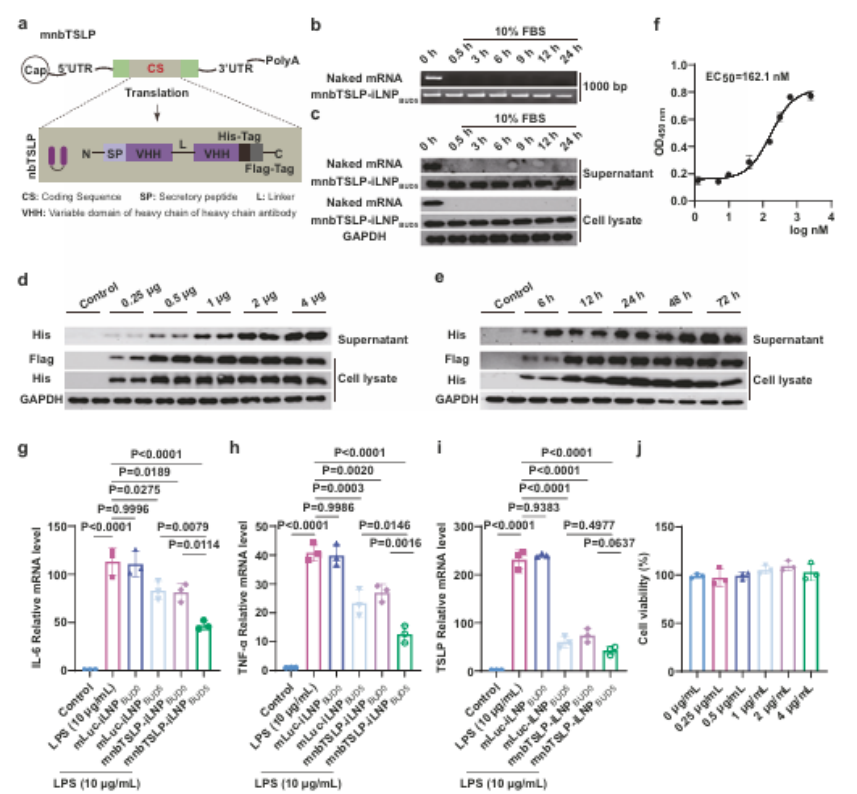
圖例5:mnbTSLP的設(shè)計(jì)與體外功能驗(yàn)證
5.mnbTSLP-iLNPBUD5緩解OVA誘導(dǎo)的急性哮喘氣道損傷
模型構(gòu)建:第 1、7��、14天腹腔注射OVA+明礬致敏��,第21-27天每日鼻內(nèi)注射50μg OVA激發(fā)���。
給藥方法:每次OVA激發(fā)前6小時(shí)�����,吸入給藥(mLuc-iLNPBUD0���、Pulmicort���、mLuc-iLNPBUD5、mnbTSLP-iLNPBUD0�����、mnbTSLP-iLNPBUD5)�����,健康組給予PBS����。
在OVA誘導(dǎo)急性哮喘模型中,研究團(tuán)隊(duì)發(fā)現(xiàn)mnbTSLP-iLNPBUD5顯著降低了氣道壁厚度����、炎癥浸潤、黏液分泌及膠原沉積���,指標(biāo)接近健康組�,優(yōu)于單藥治療。
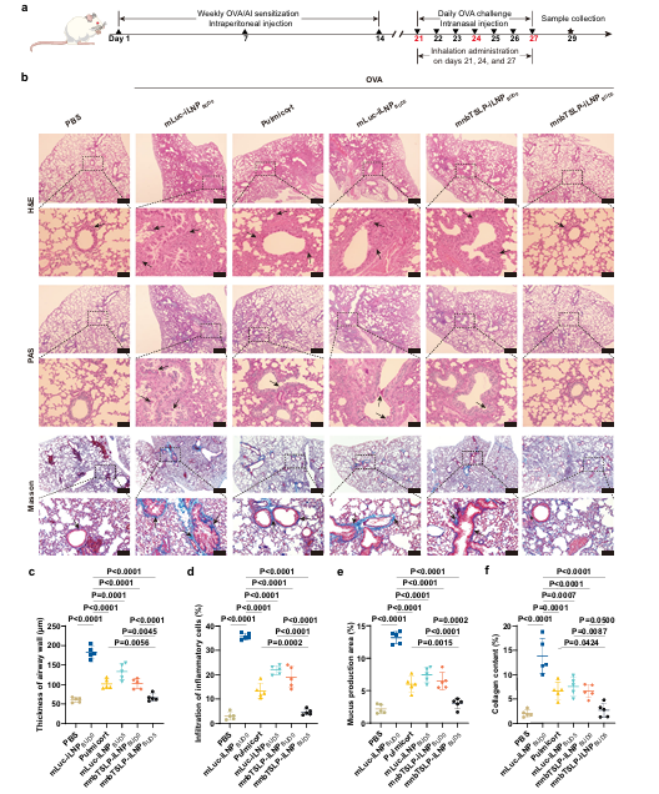
圖例6:mnbTSLP-iLNPBUD5緩解OVA誘導(dǎo)的急性哮喘氣道損傷
6.mnbTSLP-iLNPBUD5改善重癥哮喘的氣道炎癥與肺功能
模型構(gòu)建: OVA+明礬致敏+高劑量OVA激發(fā)
給藥方法:通過吸入方式給予對應(yīng)制劑�����,單次mRNA劑量30μg����,布地奈德劑量按分組設(shè)定����。
而在OVA誘導(dǎo)重癥哮喘模型中,研究團(tuán)隊(duì)發(fā)現(xiàn)mnbTSLP-iLNPBUD5 組的BALF炎癥細(xì)胞�、血清IgE及炎癥因子水平大幅降低;氣道對乙酰甲膽堿反應(yīng)平緩�����,AHR 癥狀顯著緩解��,肺功能改善明顯���。
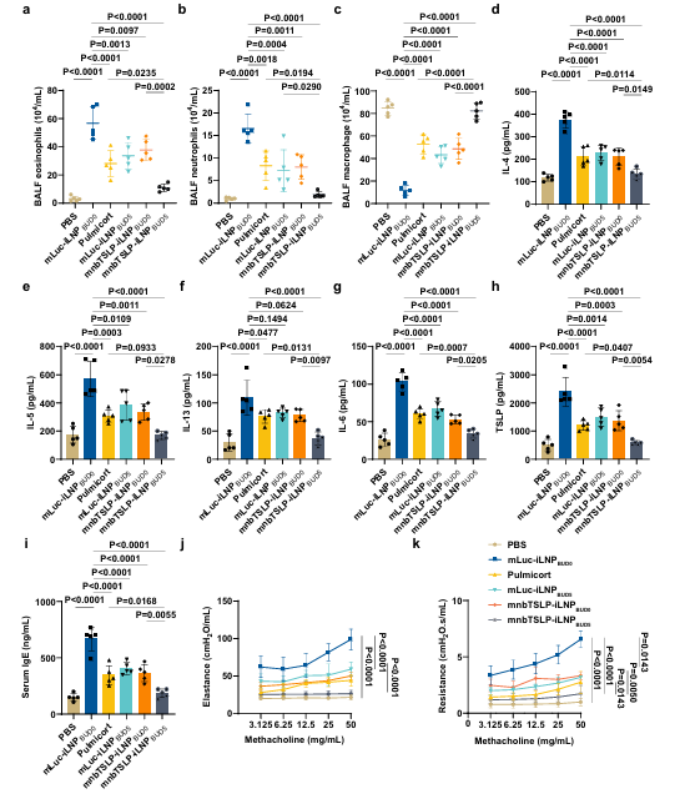
圖例7: mnbTSLP-iLNPBUD5改善重癥哮喘的氣道炎癥與肺功能
7.mnbTSLP-iLNPBUD5在類固醇抵抗性哮喘中的協(xié)同治療作用
模型構(gòu)建:第 1�、7、14天腹腔注射OVA+明礬致敏���,第21-70天每周3次鼻內(nèi)注射20μg OVA+10μg TSLP激發(fā)�����。
給藥方法:第56-70天���,每周1次給藥,mnbTSLP-iLNP系列制劑通過吸入給予���,Tezepelumab經(jīng)尾靜脈注射(70μg /次)����,其他對照組按對應(yīng)方式給藥�。
在OVA/TSLP誘導(dǎo)類固醇抵抗性哮喘模型中,研究團(tuán)隊(duì)發(fā)現(xiàn)布地奈德單藥無效��,mnbTSLP-iLNPBUD5可維持低氣道阻力�����,抑制炎癥與重塑���,降低p-STAT3/p-p38水平�,恢復(fù)藥物敏感性。

圖例8:mnbTSLP-iLNPBUD5在類固醇抵抗性哮喘中的協(xié)同治療作用
8.mnbTSLP-iLNPBUD5的體內(nèi)安全性評估
連續(xù)吸入給藥后�,小鼠體重、生化指標(biāo)�、血常規(guī)無異常,心肝腎脾無病理改變����,全身安全性良好。
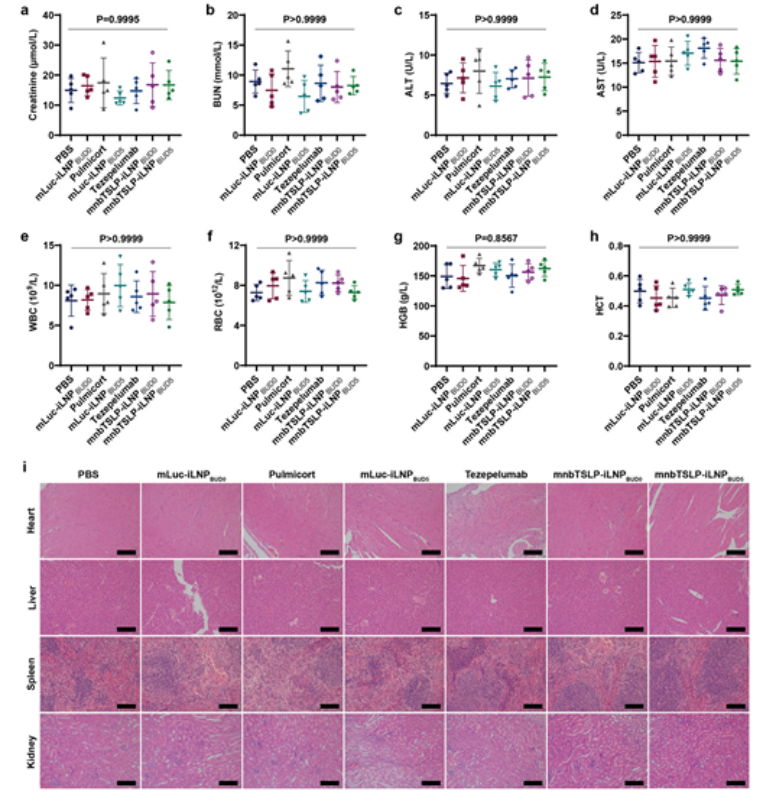
圖例9:mnbTSLP-iLNPBUD5的體內(nèi)安全性評估
知識分享:研究亮點(diǎn)
1 通過組分配方�����、制備工藝�����、霧化體系等研究變量的多維度協(xié)同優(yōu)化�����,并在此基礎(chǔ)上整合抗哮喘甾體藥物為結(jié)構(gòu)成分����,構(gòu)建新型吸入式mRNA-LNP體系,實(shí)現(xiàn)小分子和核酸藥物針對肺部的精準(zhǔn)遞送�����;
2 協(xié)同抗炎作用:依托載體與核酸藥物的協(xié)同效應(yīng)�����,顯著抑制氣道炎癥及TSLP信號通路�����,聯(lián)合療法顯著減輕小鼠模型的氣道炎癥���、重塑和高反應(yīng)性���,且mnbTSLP通過抑制關(guān)鍵炎癥通路,恢復(fù)哮喘小鼠對布地奈德的敏感性�;
3 患者依從性高:該策略采用非侵入性吸入給藥,操作簡便�����,患者接受度高����,具有廣闊的臨床應(yīng)用前景�。
參考文獻(xiàn):
Nature Communications ( IF15.7 ) Pub Date :2025-07-01,DOI: 10.1038/s41467-025-61114-4.
 歡迎來到蘇州艾特森制藥設(shè)備有限公司網(wǎng)站!
歡迎來到蘇州艾特森制藥設(shè)備有限公司網(wǎng)站! 歡迎來到蘇州艾特森制藥設(shè)備有限公司網(wǎng)站!
歡迎來到蘇州艾特森制藥設(shè)備有限公司網(wǎng)站!










